Thứ Năm, ngày 03/10/2019 16:22 PM (GMT+7)
Cục Quản lý Dược, Bộ Y tế vừa có công văn về việc thu hồi thuốc chứa Ranitidine có chứa tạp chất vượt giới hạn cho phép.
Theo Cục Quản lý Dược, 11 loại thuốc trên là thuốc điều trị viêm loét dạ dày và ruột có chứa hoạt chất ranitidine. Lý do thu hồi là trong thuốc chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư ở hàm lượng vượt quá ngưỡng cho phép của quốc tế.
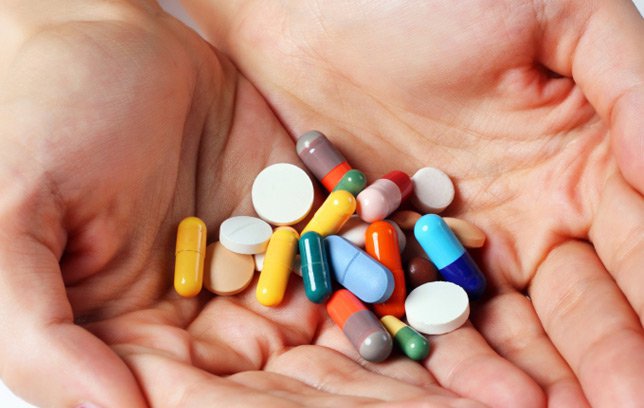
11 loại thuốc trên là thuốc điều trị viêm loét dạ dày và ruột có chứa hoạt chất ranitidine.
Theo quy định, giới hạn NDMA không quá 0.32 ppm (tính trên liều chấp nhận tối đa của NDMA là 96 nanogram/ngày và liều sử dụng tối đa của ranitidine là 300mg/ngày).
11 loại thuốc thu hồi có hàm lượng ranitidine 150 mg/10ml, 150 mg/25 ml và loại 150 mg, xuất xứ từ Ấn Độ, Tây Ban Nha, Italia, Anh, Thái Lan, Malaysia.
Trước đó, cơ quan khoa học y tế Singapore (HSA), cơ quan quản lý dược phẩm Thụy Sĩ (Swissmedic) cũng đã thu hồi 11 thuốc nói trên.
Hiện Cục Quản lý Dược đã yêu cầu các công ty nhập khẩu thuốc phối hợp với nhà phân phối thuốc thông báo thu hồi tất cả lô thuốc thành phẩm này.
11 loại thuốc thu hồi có hàm lượng ranitidine (tạp chất gây ung thư) bao gồm: - Aciloc 150 và 300 - Công ty Cadila Pharmaceuticals Ltd. (Ấn Độ)
- Apo-Ranitidine 150mg - Apotex Inc. (Canada)
- Zantac Tablets - Glaxo Wellcome S.A (Tây Ban Nha)
- Zantac Injection - GlaxoSmithKline Manufacturing S.p.A (Italy)
- Ratylno-150 - Micro Labs Ltd (Ấn Độ)
- Hyzan Tablet 150mg - Xepa - Soul Pattinson (Malaysia)
- Neoceptin R-150 Tablet 150mg - của Beximco Pharmaceuticals Ltd.
-Vesyca film coated tablet 150mg - Y.S.P. Industries (Malaysia)
- Xanidine Tablet 150mg - Berlin Pharmaceutical Industry Co. Ltd. (Thái Lan)
- Zantac Syrup 150mg/10ml - Aspen Bad Oldesloe GmbH ( Đức)
- Glaxo Wellcome Operations (Mỹ).
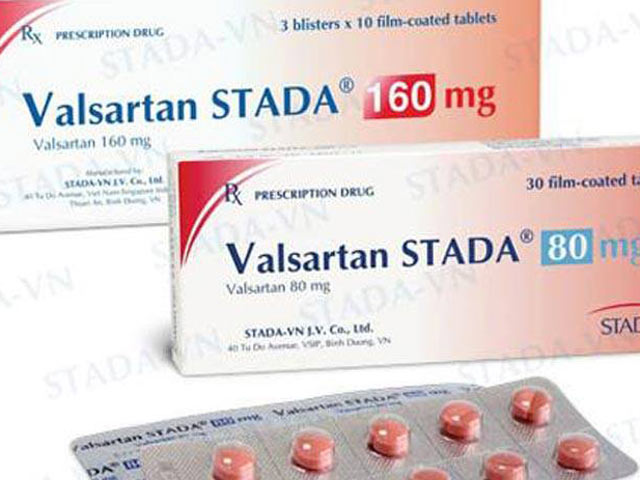
Liên quan tới lùm xùm về việc thu hồi thuốc tim mạch có chứa chất gây ung thư, Cục Quản lý Dược, Bộ Y tế vừa quyết...
No comments:
Post a Comment